阿尔茨海默病是一种神经退行性疾病,其特征是毒性肽淀粉样蛋白-β (Aβ)在脑内的错误沉积、并伴有突触缺失进而产生认知障碍。减少Aβ积累或维持突触密度可以维持阿尔茨海默病患者的正常认知功能。TRPM7是一种独特的离子通道,其C末端包含一个激酶结构域。研究表明TRPM7与神经退行性疾病相关。然而,目前TRPM7是如何参与此类疾病的病理过程仍是未解之谜。
2023年7月11日,复旦大学脑科学研究院那德(Nashat Abumaria)课题组在《Science Signaling》上发表了一项相关的科学研究。该项研究首先证明了阿尔茨海默病患者和两种阿尔茨海默病模型小鼠的海马组织(参与学习和记忆过程的关键大脑区域)中的TRPM7表达量显著降低。随后,作者发现上调TRPM7或者其激酶结构域的表达量可抵消Aβ的病理毒性。并揭示TRPM7激酶结构域是如何减少脑内Aβ的沉积,并保护突触密度,进而修复阿尔茨海默病模型小鼠的记忆缺陷的(图1)。
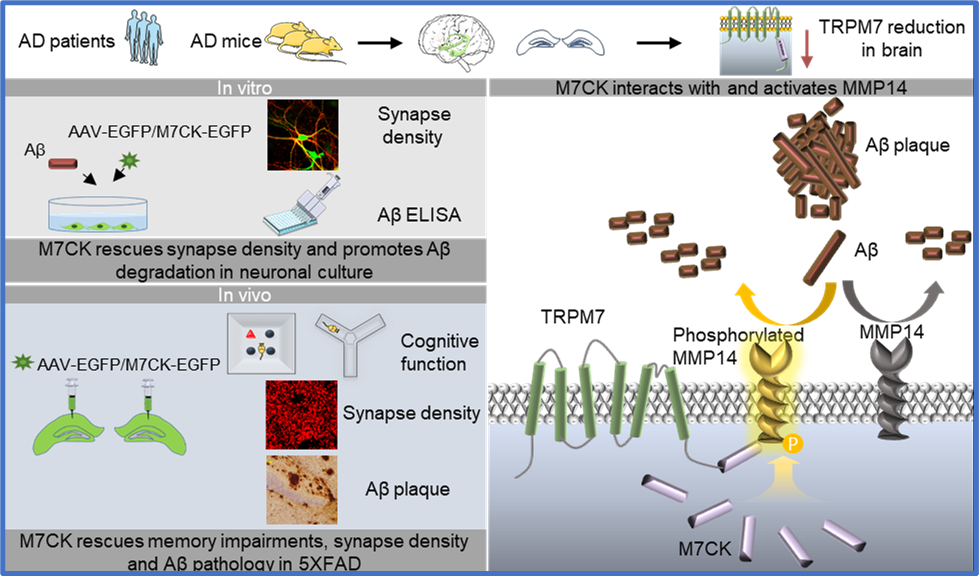
图1. 研究概述(Aβ:淀粉样蛋白-β;AD:阿尔茨海默病; M7CK:TRPM7的激酶结构域)
本研究在阿尔茨海默病患者的脑样本中观察到TRPM7的表达减少后,那德课题组进一步研究发现在两种阿尔茨海默病模型小鼠的海马体中TRPM7的表达量也显著下降。在小鼠海马原代神经元培养中,作者还发现全长的TRPM7或其功能性激酶结构域(M7CK)的过表达阻止了Aβ对突触的毒性。而且,单独过表达TRPM7的离子通道部分或激酶活性被抑制的TRPM7突变体不具有相同的保护作用。
TRPM7的功能激酶结构域在不同年龄的阿尔茨海默病的年轻(5-6个月)和老年(14个月)模型小鼠的海马体中过表达可以分别预防和逆转其记忆缺陷。其激酶结构域能够有效修复其脑内突触密度,并减少其海马体中的淀粉样蛋白沉积。
在原代神经元培养和小鼠脑中,作者还发现TRPM7的激酶结构域与MMP14(一种参与降解Aβ的金属蛋白酶)相互作用并将其激活。TRPM7的激酶结构域对淀粉样蛋白的沉积的影响是通过其激酶段直接激活蛋白酶MMP14的活性所介导的,并通过MMP14促进其脑内Aβ的降解和清除。
这项研究表明,TRPM7在神经退行性疾病病理过程中表达量下降,并揭示了TRPM7通过参与降解Aβ进而影响阿尔茨海默病病理进程的科学机制。这种科学机制可能是阿尔茨海默病领域在基础研究和治疗应用水平上的概念进步。
来自复旦大学脑科学研究院那德课题组的博士生张诗萌和曹霏霏是该论文的共同第一作者。来自复旦大学脑科学研究院的那德(Nashat Abumaria)研究员和李薇副研究员是该论文的共同通讯作者。来自中国科学院IRCBC的王文元研究员和陈椰林研究员为本课题提供了5XFAD的模型小鼠。这项工作得到了国家自然科学基金(NSFC)、上海市科技重大专项、张江(ZJ)实验室和上海市脑科学与类脑技术中心的支持。