

2025年10月15日,《Journal of Clinical Investigation》在线发表了题为《3D培养的人源中型多棘神经元能够功能性整合进亨廷顿病小鼠的神经环路并改善其运动缺陷》(3D-cultured human medium spiny neurons functionally integrate and rescue motor deficits in Huntington’s disease mice)的研究论文。研究首次建立了人多能干细胞高效定向分化为纹状体中型多棘神经元(MSN)亚型的三维悬浮培养新技术,分化的细胞在分子特征上与胎脑内源神经元高度相似;移植实验进一步证实,这些来源于人多能干细胞的MSN亚型能够在结构与功能层面整合入亨廷顿病(Huntington’s Disease, HD)模型小鼠的基底神经节环路的直接通路和间接通路,显著改善HD小鼠的运动功能障碍,为基于神经环路重建的HD的细胞替代治疗提供了全新技术途径和理论基础。

亨廷顿病(Huntington’s disease, HD)是一种常染色体显性遗传性神经退行性疾病,全球发病率约为每十万人5–10例,通常在中年起病并持续进展。该病由HTT基因中CAG重复序列异常扩增引起,导致纹状体中型多棘神经元(medium spiny neurons, MSNs)特异性退变,表现为舞蹈样运动障碍、认知功能下降及精神行为异常。目前尚无能够逆转病程的治疗手段,现有药物治疗仅能缓解症状,难以阻止神经元丢失的持续进展。
MSNs是纹状体的主要神经元类型,约占该区神经元总数的85%-95%(不同物种略有差异),可分为D1-MSN(参与直接通路)和D2-MSN(参与间接通路)两大亚群,分别投射至苍白球内侧部(GPi)、黑质网状部(SNr)及苍白球外侧部(GPe),在运动、奖赏及认知调控中发挥关键作用。利用人多能干细胞(hPSCs)分化获得MSN亚型,为解析HD发病机制及开发细胞替代疗法提供了新的可能。然而,现有分化方法效率低,重复性和稳定性差,得到的MSNs亚型不明确。因此,建立高效稳定的MSN特异性分化方法,并验证其在HD模型中的神经环路整合与功能恢复能力,具有重要科学意义和临床价值。
研究团队建立了一种无血清无异种成分的全程三维悬浮分化新技术,在无需外源SHH信号通路激动剂的情况下,该体系即可自激活该信号通路,高效生成纹状体神经前体细胞(LGE神经祖细胞),研究团队将该体系命名为3D-default XFSC(图1)。
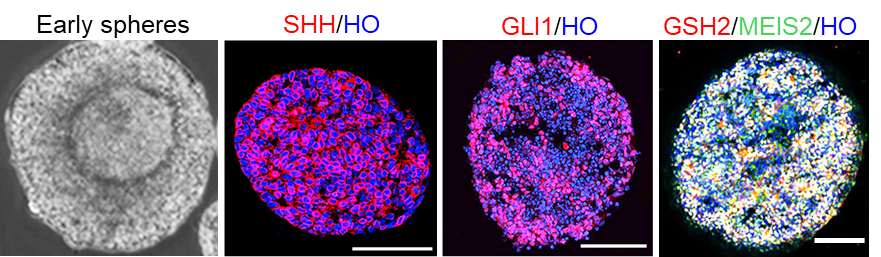
图1 3D-default XFSC系统可自分泌SHH诱导产生LGE祖细胞
为评估3D-default XFSC衍生细胞的体外分化效率及身份属性,研究团队通过多种成熟MSN亚型标志物的多重染色及单细胞测序证明,该方法可高效获得与人胎脑来源MSN祖细胞及神经元亚型高度相似的功能性神经元(图2)。
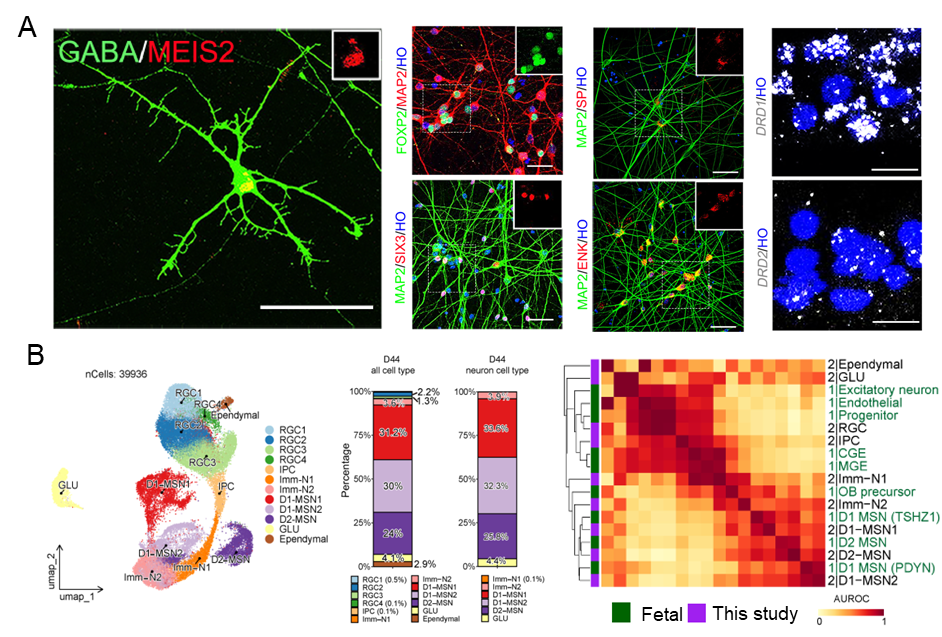
图2 3D-default XFSC可衍生不同MSN亚型并与胎脑来源纹状体细胞转录组高度相似
为进一步验证3D-default XFSC获得MSN细胞在体内的神经环路整合特异性与功能,研究团队将分化获得的人源LGE神经前体细胞移植至HD模型小鼠纹状体。单细胞转录组分析显示,移植细胞与人类胎脑对应神经元亚型具有高度转录相似性(图3A)。免疫组化结果进一步表明,移植细胞长期存活并分化为D1-和D2-MSN亚型,其轴突投射至宿主苍白球与黑质网状部等经典靶区(图3C)。行为学测试结果显示,移植3D-default XFSC衍生细胞可显著改善HD模型小鼠运动功能,表明该细胞药物具备良好的环路重建能力与治疗潜力。
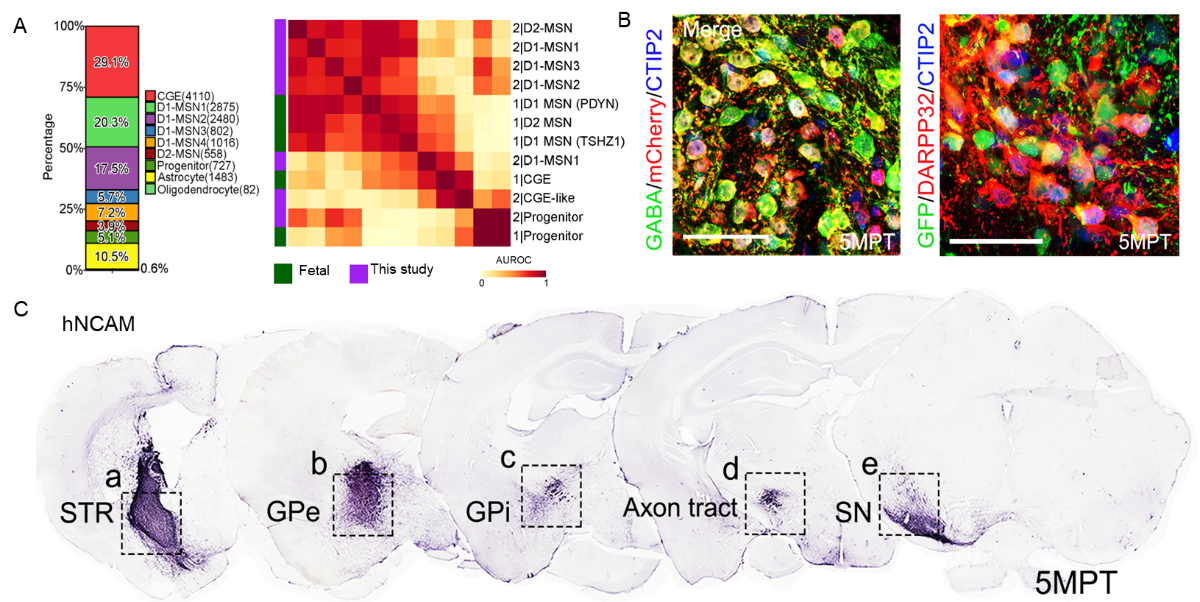
图3 3D-default XFSC来源祖细胞在HD模型脑内分化成熟为不同MSN亚型,并投射至内源靶标区域
总结:该研究建立的3D无血清无异种成分的临床级悬浮分化新体系,能够实现高效、稳定的人源MSN亚型的特异性分化。移植后,这些细胞可长期存活,分化为多种MSN亚型,并成功整合入宿主神经环路,从而显著改善亨廷顿病模型小鼠的运动功能。该成果为解析纹状体神经元发育机制及推动亨廷顿病等神经退行性疾病的细胞替代治疗提供了关键技术路径与实验基础。
复旦大学脑科学研究院熊曼研究员为最后通讯作者,中国科学院脑智卓越中心陈跃军研究员为共同通讯作者。复旦大学脑科学研究院梅玉婷硕士(儿科联合培养)、许愿硕士、中国科学院脑智卓越中心章馨月博士为该论文的共同第一作者。复旦大学肖雷研究员、意大利米兰大学Elena Cattaneo教授为该研究提供了重要帮助。复旦大学脑科学研究院李缘博士、彭星升硕士、程倩博士等,中国科学院脑智卓越中心周盈盈博士、谢连顺博士等为本研究做出了重要贡献。该研究得到了国家自然科学基金优秀青年基金、科技部重点研发、上海市科委等项目的资助。
原文链接:https://doi.org/10.1172/JCI187941








 公共技术平台网上预约
公共技术平台网上预约
