

腺苷酸环化酶(ACs)是一类具有重要生理学功能的酶家族,可以催化ATP生成胞内第二信使cAMP。迄今为止,哺乳动物体内共发现10个亚类的ACs。鉴于ACs的广泛分布和参与众多细胞生理过程,研究AC亚型在不同类型组织细胞中的功能从而探索靶向AC亚型的临床药物开发是大有前景和极具挑战的工作。相对于其他AC亚型,对AC3在神经系统的功能研究相对较晚。最初的研究发现AC3主要表达在嗅上皮纤毛,负责嗅球气味和信息素的检测,激素或气味分子与G蛋白耦联受体(GPCRs)相互作用通过Gαolf蛋白激活AC3。敲除AC3会导致气味介导的信号通路缺失,气味介导的学习等行为受损,嗅觉轴突发育及投射异常,嗅觉纤毛对气流机械力的检测缺失。随后的研究发现AC3在整个中枢神经系统神经元的初级纤毛广泛表达,并被作为中枢神经元初级纤毛的标志物。AC3全身敲除小鼠出现对新物体的短期记忆减弱,环境条件恐惧记忆消失,并出现睡眠模式改变和抑郁样行为等。张玉秋课题组的最新研究发现,不同于中枢神经系统和嗅觉感受器,AC3在躯体感觉感受器神经元特别是DRG伤害感受器神经元胞体大量表达。利用cre-loxp系统选择性敲除DRG内AC3(AC3CKO),小鼠对多种方式的伤害性刺激包括机械、热和化学刺激的反应增强,表明DRG缺失AC3导致痛觉敏化。电生理记录显示,敲除AC3的DRG神经元电压门控钾通道电流(IA和IK)降低,神经元兴奋性增强。作为代偿,AC3CKO小鼠DRG内AC1表达显著上调,cAMP含量增加。抑制AC1可显著翻转AC3CKO引起的cAMP浓度增高、电压门控钾电流减小和神经元兴奋性增强,并有效缓解AC3CKO小鼠的痛觉敏化行为。
腺苷酸环化酶(ACs)是G蛋白耦联受体(GPCRs)的效应器。阿片类药物是一种常见的镇痛药物,可通过其相应G蛋白耦联受体激活Gαi蛋白,抑制ACs催化生成cAMP,减少突触传递,降低神经元活动,抑制伤害性行为反应。作为DRG神经元主要表达的AC亚型,AC3是否参与介导阿片类药物的镇痛作用尚缺乏实验证据。本研究结果显示,AC3CKO导致κ阿片受体(KOR)介导的镇痛作用完全缺失,但对μ阿片受体(MOR)和δ阿片受体(DOR)介导的镇痛无影响。鞘内给予Gαi/o 蛋白抑制剂可完全阻断KOR介导的镇痛效应。RNAscope荧光原位杂交实验显示,超过85%以上的KOR阳性神经元表达AC3 mRNA。邻位连接技术和免疫共沉淀实验显示KOR和AC3存在相互作用,蛋白对接模型预测显示,KOR分子上的170Arg-196Leu α-螺旋结构与AC3的940ILE-952LEU β-turn结构和1123Asp-1142asp α--螺旋结构相结合。这些结果提示,除了经典的Gαi/o信号通路,KOR与AC3蛋白之间直接的相互作用可能也参与介导κ阿片镇痛。
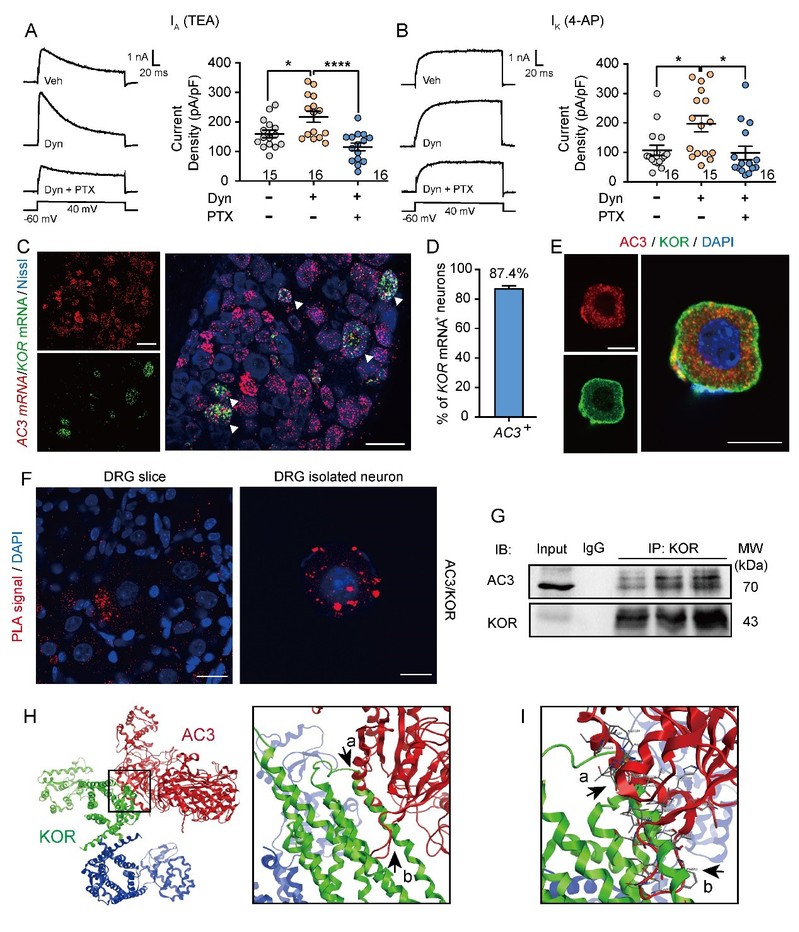
图1. AC3与KOR的之间的相互作用
该项研究揭示了小鼠外周神经系统AC3在伤害性信息调控及KOR阿片镇痛中的关键性作用,为开发靶向特异性AC亚型的镇痛策略提供了重要线索。
该项研究成果主要由张玉秋教授课题组博士生张雯雯(第一作者)完成,山东中医药大学付先军教授课题组提供蛋白对接模型。相关研究成果以“Peripheral ablation of type Ⅲ adenylyl cyclase induces hyperalgesia and eliminates KOR-mediated analgesia in mice”为题,发表于JCI Insight(2022,7:e153191)杂志上。研究得到教育部脑科学前沿科学中心和医学神经生物学国家重点实验室,以及张江实验室和上海脑科学与类脑研究中心支持。
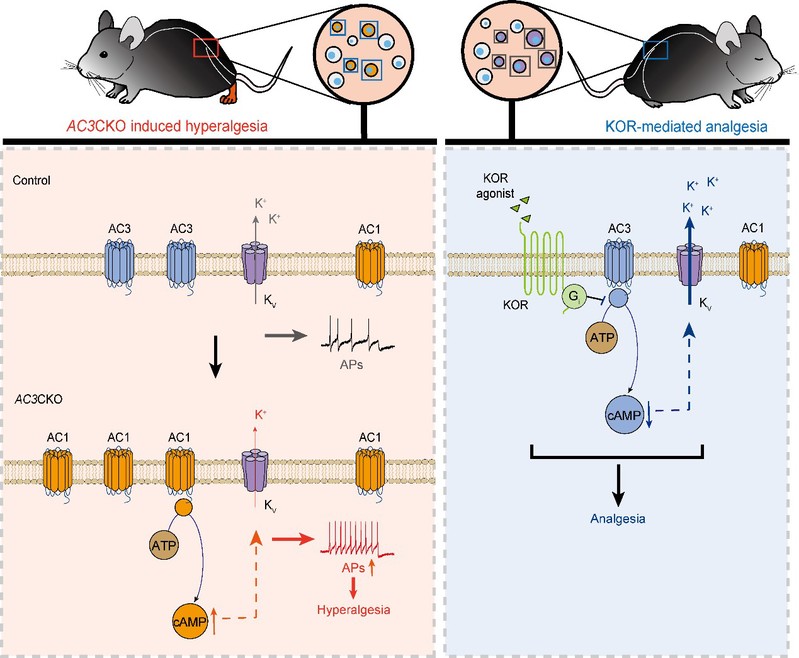
总结示意图








 公共技术平台网上预约
公共技术平台网上预约
